Le cortège électronique de l’atome.
La structure électronique que nous représentions avec les lettres K, L, M, ... etc. n'est plus utilisée en seconde depuis 2020. A la place nous utiliserons une représentation plus moderne s'appuyant sur la théorie quantique. Désormais on parlera de sous-couches s, p, d, ... etc. L'étude se limitera aux atomes dont le numéro atomique Z ≤ 18. On rappelle également que puisque un atome est électriquement neutre, le nombre d'électrons est égal au nombre de protons (Z).
1. Sous-couches électroniques s, p, d, ...
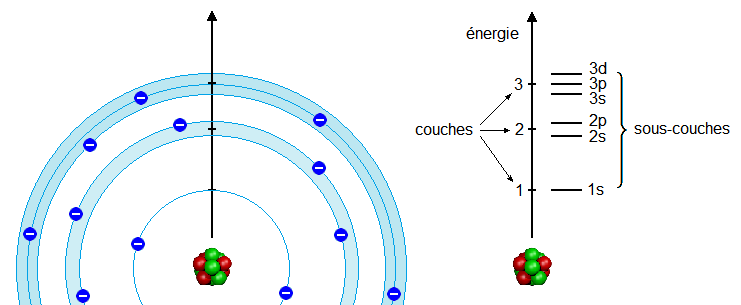
L'étude des électrons d'un atome a montré que ceux-ci se répartissaient en couches (1, 2, 3, ...), qui se divisaient elles-mêmes en sous-couches (s, p, d, ...) comme le montre le schéma ci-dessus :
Les électrons appartiennent à des sous-couches que nous nommons "s, p, d, ...".
Pour préciser à quelle couche appartient une sous-couche, nous écrivons le numéro de la couche devant
la lettre de la sous-couche.
Par exemple la sous-couche "p" de la couche "2" s'écrira : "2p".
Remarquez que la couche "1" ne contient qu'une sous-couche, la couche "2" en contient 2, la couche "3"
en contient 3, ...
L'énergie d'une sous-couche est quantifiée (elle a une valeur précise).
Par exemple, on voit que les électrons de la sous-couche 2s ont plus d'énergie que ceux
de la couche 1s.
Retenez simplement qu'en écrivant les sous-couches dans l'ordre conventionnel d'énergie croissante,
nous aurons : 1s, 2s, 2p, 3s, 3p, 3d, ...
2. Remplissage des sous-couches par les électrons
Pour remplir correctement les sous-couches électroniques, vous devez connaître le nombre maximum d'électrons à placer dans chaque sous-couches :
s est pleine avec 2 électrons.
p est pleine avec 6 électrons.
Ensuite, vous devez savoir que le remplissage s'effectue dans l'ordre 1s, 2s, 2p, etc.
on ne passe à la sous-couche suivante que lorsque la précédente est pleine.
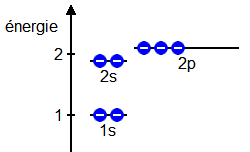 Exemple avec l'atome d'azote (Z = 7) :
Exemple avec l'atome d'azote (Z = 7) :
1) Nous remplissons totalement la sous-couche 1s avec 2 électrons.
Il reste donc 7 - 2 = 5 électrons à placer.
2) Nous remplissons totalement la sous-couche 2s avec 2 électrons.
Il ne reste plus que 5 - 2 = 3 électrons disponibles.
3) Nous plaçons ces 3 derniers électrons dans la sous-couche 2p
qui n'est alors que partiellement remplie.
3. Structure électronique
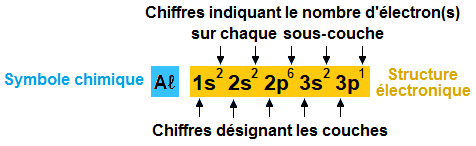
Par convention nous écrivons le nombre d'électrons présent dans la sous-couche juste en haut
et à droite de la lettre représentant cette sous couche.
Vous trouverez ci-dessous une excellente video concernant le cours :
Exercice 1 : En vous aidant de l'exemple vu dans la partie 2, écrire la structure électronique de l'atome d'azote.
4. Couche de valence
Définitions de la couche de valence :
La couche de valence est la dernière couche électronique partiellement ou totalement remplie.
Exemple pour l'aluminium, la dernière couche est la couche n°3. Elle contient la structure 3s2 et
3p1.
Le nombre total d'électrons appartenant à cette couche est donc de 2 + 1 = 3
On écrira que la couche de valence de l'atome d'aluminium contient 3 électrons.
Ce nombre d'électrons de la couche de valence est très important car :
C'est le nombre d'électrons de la couche de valence qui définit les propriétés chimique de l'élément.
Exercice 2 :
1) Quelle est la couche de valence de l'atome d'azote ?
2) Combien d'électrons au total possède cette couche ?
5. Cas particulier de l'ion
La difficulté ici est de recenser le nombre d'électrons de l'ion sachant qu'il ne correspond plus
au nombre de protons (Z).
Exemple avec l'ion Magnésium Mg2+ :
C'est un atome qui a perdu 2 électrons (en perdant 2 charges négatives l'atome se retrouve avec un
excédant de 2 charges positives).
Le numéro atomique du Magnésium est 12, donc le nombre d'électrons de l'ion magnésium est 12 - 2 = 10
Vérifiez alors que sa structure électronique s'écrit : 1s2 2s2
2p6
Exercice 3 :
1) Combien d'électrons possède l'ion Chlorure (Cl-) ?
2) Ecrire la structure électronique de l'ion Chlorure.
Donnée : Atome de chlore Z = 17
La sous-couche 1s est pleine avec 2 électrons.
La sous-couche 2s est pleine avec 2 électrons.
La sous-couche 2p est pleine avec 6 électrons.
La sous-couche 3s est pleine avec 2 électrons.
La sous-couche 3p est partiellement remplie avec 1 électron.