Représentation des molécules par une formule brute
1. Définition
La formule brute permet de connaître le type et le nombre d'atomes contenu dans une molécule. Par contre elle ne permet pas de connaître la disposition spatial des atomes. C'est la formule que vous utilisez depuis le collège.
Une formule brute s'écrit en juxtaposant les noms des éléments chimiques, et en indiquant en indice le nombre de chaque élément lorsqu'il est supérieur à un.
Exemple : H2O, CO2, CH4, NH3, etc.
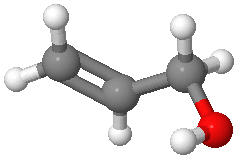 Pour mieux comprendre, examinons en détails cette molécule d'alcool allylique :
Pour mieux comprendre, examinons en détails cette molécule d'alcool allylique :
Elle comporte :
- 3 atomes de carbone (atomes gris foncés).
- 6 atomes d'hydrogène (atomes blanc).
- 1 atome d'oxygène (atome rouge).
La formule brute de l'alcool allylique s'écrit donc :
C3H6O
Remarque : Il n'y a pas d'ordre pour nommer les atomes. On peut donc l'écrire aussi bien :
H6OC3 ou OH6C3
 Attention : Bien écrire les nombres en indice (petite taille en bas à droite de l'élément).
En effet, CO2 signifie une molécule de dioxyde de carbone
(composée d'un atome de carbone et de deux atomes d'hydrogène), alors que 2CO signifie deux molécules de monoxyde
de carbone (composée chacune d'un seul atome de carbone et d'un seul atome d'oxygène).
Attention : Bien écrire les nombres en indice (petite taille en bas à droite de l'élément).
En effet, CO2 signifie une molécule de dioxyde de carbone
(composée d'un atome de carbone et de deux atomes d'hydrogène), alors que 2CO signifie deux molécules de monoxyde
de carbone (composée chacune d'un seul atome de carbone et d'un seul atome d'oxygène).
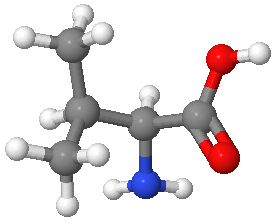
Exercice 1 : La valine représentée ci-contre fait partie des 9 acides aminées essentiels pour l'homme.
1) Combien y-a-t'il d'atomes de carbone (gris foncé) dans cette molécule ?
2) Combien y-a-t'il d'atomes d'hydrogène (blanc) ?
3) Combien y-a-t'il d'atomes d'azote (bleu) ?
4) Combien y-a-t'il d'atomes d'oxygène (rouge) ?
5) Déduire des questions précédentes la formule brute de la valine.
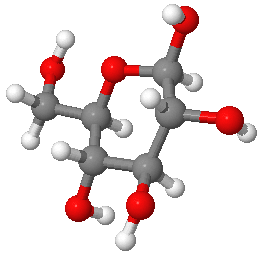
Exercice 2 : Le diabète apparaît lorsque le corps n'est plus en mesure d'éliminer l'excès de glucose
dans le sang (voir la molécule de glucose ci-contre).
Quelle est la formule brute du glucose ?
2. Formules brutes et équation chimique
Les formules brutes sont fréquemment utilisées dans l'écriture des équations chimiques. Par exemple :
C + O2 → CO2 ou encore
CH4 + 2O2 → 2H2O + CO2
Exercice 3 : La réaction chimique d'une molécule de dioxygène (O2) avec deux molécules de
dihydrogène (H2) donne deux molécules identiques.
1) Pourriez vous trouver la formule brute de cette molécule inconnue ?
2) Ecrire l'équation chimique complète de cette réaction