
Physique Chimie en seconde
L'atome
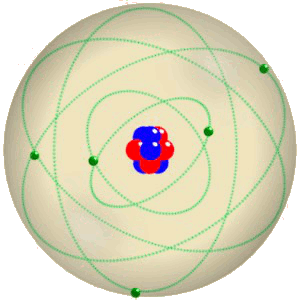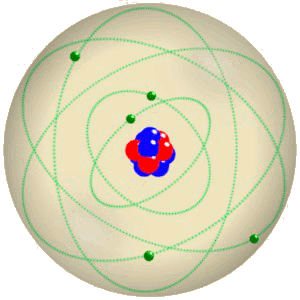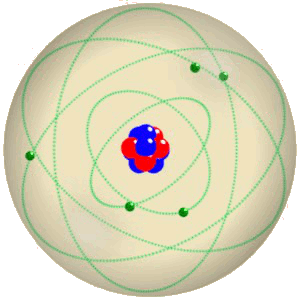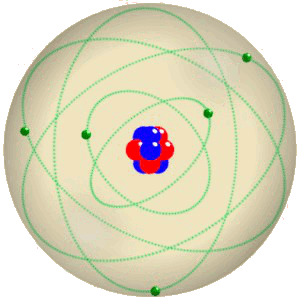
Un atome
1. Les atomes de l'Univers
Au centre de l'atome se trouve le noyau, un agglomérat de
• protons, et de
• neutrons.
Autour du noyau orbitent les électrons.
Toute la matière de l'Univers (étoiles, planètes, plantes et animaux)
est faite d'atomes, dont les dimensions sont approximativement :
• 10-10 m pour le diamètre de la zone de circulation des électrons.
• 10-15 m pour le diamètre du noyau.
2. Expérience de Rutherford
Cette expérience consistait à projeter des particules α à travers une mince feuille d'or. Des plaques photographiques disposées en cercle au tour de la feuille, permettaient ensuite de visualiser les impacts des particules après la collision avec l'or.

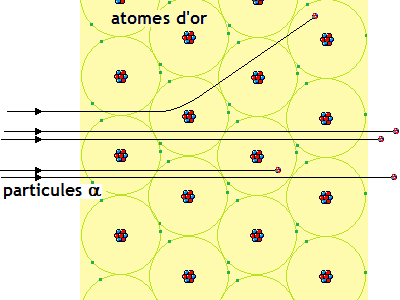
Cette expérience a montré que presque toutes les particules traversaient la feuille d'or sans subir de déviation. En conclusion, si les particules ne rencontraient pas de matière sur leur trajet, c'est que :
l'atome est essentiellement constitué de vide (absence de matière).
Il n'y a rien entre le noyau et les électrons.
3. Protons, neutrons et électrons
Protons et électrons sont des particules chargées de la même quantité d'électricité, mais de signes inverses (un proton contient une charge positive, et un électron une charge négative). Ce sont les charges connues à ce jour, les plus petites qui existent. L'unité de charge est le "Coulomb" (C). Les masses des protons et des neutrons sont sensiblement identiques. Le tableau ci dessous résume l'essentiel :

| Nom des particules | Nucléons | Electrons | |
| Neutron | Proton | ||
| Masse (en kg) | 1,675 × 10-27 | 1,673 × 10-27 | 9,109 × 10-31 |
| Charge (en C) | Aucune | + 1,6 × 10-19 | - 1,6 × 10-19 |
4. Écriture symbolique du noyau d'un atome.
Par convention l'écriture symbolique d'un noyau d'atome est représenté de la façon suivante :
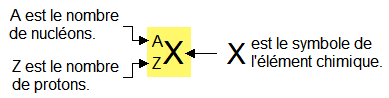
X est le symbole chimique. Ce que nous avons l'habitude d'écrire en abrégé avec une ou plusieurs lettres : C, Fe, O, etc.
Exemple de quelques symboles chimiques fréquemment utilisés au lycée :
| Élément | Hydrogène | Carbone | Azote | Oxygène | Sodium | Magnésium | Chlore | Calcium | Potassium | Fer | Cuivre | Zinc |
|---|---|---|---|---|---|---|---|---|---|---|---|---|
|
Symbole
chimique |
H | C | N | O | Na | Mg | Cl | Ca | K | Fe | Cu | Zn |
Il est vivement recommandé de connaitre par coeur les 4 premiers (fond jaune).
Z est le nombre de protons présent dans le noyau de l'atome. Z est également appelé numéro atomique.
N est le nombre de neutrons présent dans le noyau, mais il ne figure pas dans l'écriture symbolique. On indique plutôt
A qui est le nombre total de nucléons (A = N + Z).
Exemple : Ecriture symbolique du noyau de l'atome de chlore :
• Cet atome contient 17 protons (cf. tableau des éléments chimiques), donc Z = 17.
• Sa forme la plus abondante dans l'Univers contient 18 neutrons, donc N = 18.
Par conséquent, nous pouvons calculer A = N + Z = 18 + 17 = 35,
et en remarquant que le symbole du chlore est Cl, on obtient :
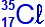
Je retiens l'essentiel :
• Z est le nombre de protons (il est aussi appelé numéro atomique).
• N est le nombre de neutrons.
• A est le nombre de nucléons (donc A = N + Z).
• X représente l'élément chimique.
5. Électroneutralité de l’atome et nombre d'électrons.
Au collège, vous avez déjà appris que :
Dans son état "normal" l'atome est électriquement neutre.
Celà signifie que le nombre de charges positives (appartenant aux protons) est égal au nombre de charges négatives (appartenant aux électrons). Par conséquent :
Dans son état "normal" l'atome contient un nombre d'électrons identique à celui du nombre de proton.
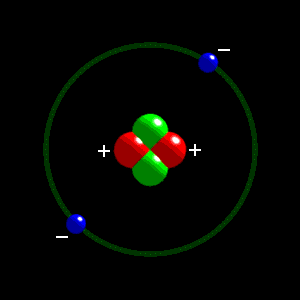
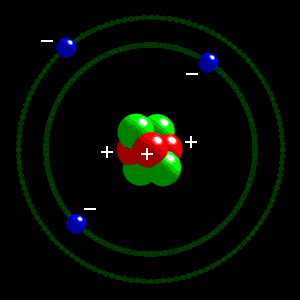
Atome d'hélium: 2 protons et 2 électrons Atome de lithium: 3 protons et 3 électrons
Objectif : A la fin de ce chapître, vous devrez
connaître la constitution d'un atome et de son noyau.
Vous devrez connaître et savoir utiliser le symbole
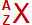 . Vous devrez savoir que
l'atome est électriquement neutre, et connaître le symbole chimique
de quelques éléments.
. Vous devrez savoir que
l'atome est électriquement neutre, et connaître le symbole chimique
de quelques éléments.