Physique Chimie en 3ème
Réactions entre solutions acides et basiques
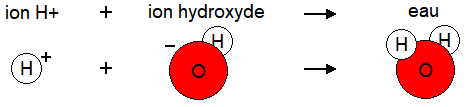
1. Réaction entre l'ion H+ et l'ion HO-
L'ion H+ (caractéristique d'un acide) réagit avec l'ion HO-
(caractéristique d'une base)
en donnant une molécule que vous connaissez très bien. Laquelle ?
Petite aide : La charge + et la charge - s'annulent ensemble. Elle n'apparaissent donc plus dans cette molécule.
Dans cette réaction l'acide et la base disparaissent.
2. Réaction entre l'acide chlorhydrique et l'hydroxyde de sodium
 Une solution aqueuse d'acide chlorhydrique contient des ions H+,
et des ions chlorure Cl-.
Une solution aqueuse d'hydroxyde de sodium contient des ions Na+ et des ions hydroxyde HO-.
Une solution aqueuse d'acide chlorhydrique contient des ions H+,
et des ions chlorure Cl-.
Une solution aqueuse d'hydroxyde de sodium contient des ions Na+ et des ions hydroxyde HO-.
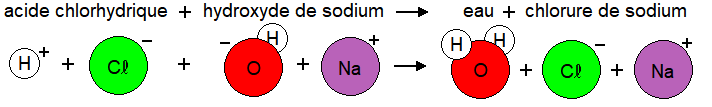
Nous savons déjà que l'ion H+ va réagir avec l'ion HO- pour donner de l'eau.
A la suite de cette réaction chimique il ne reste donc que des ions sodium et chlorure.
Écrivons l'équation :
Lorsque l'eau s'évapore, les deux ions restant se lient en donnant la molécule NaCl qui est le Chlorure de sodium que nous
appelons familièrement en cuisine du sel.
Conclusion : Cette réaction chimique donne de l'eau salée.
Attention ces réactions sont dangereuses avec des acides et des bases fortes, car pouvant donner beaucoup de chaleur et quelquefois des projections violentes.
3. Les réactions chimiques en images
Pour mieux comprendre, voici les réactions précédentes en images :